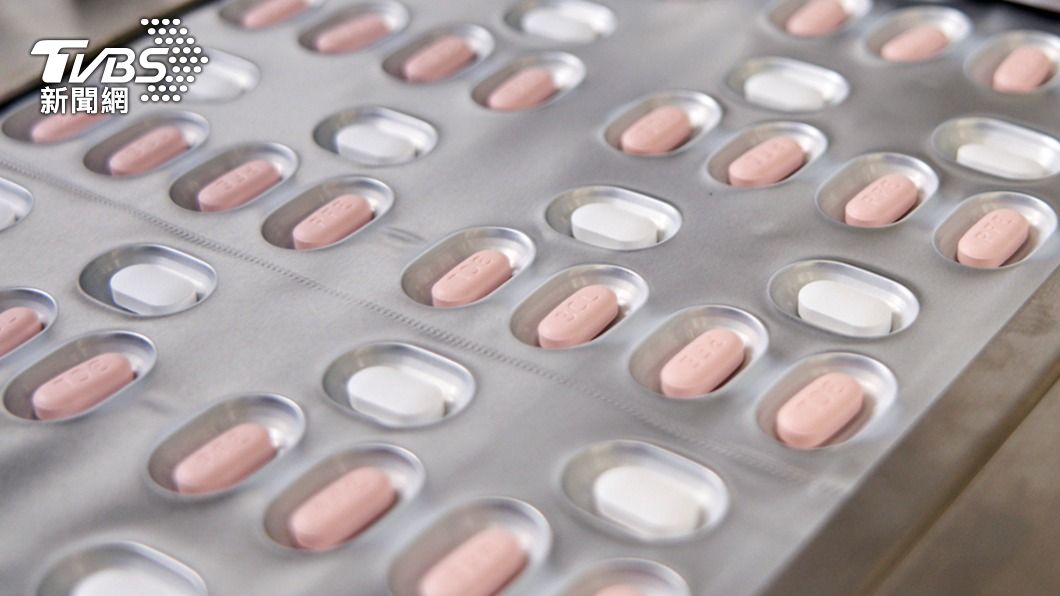
南韓食品醫藥品安全處今(27)日宣布,批准美國輝瑞藥廠研發的新冠口服藥「Paxlovid」在該國的緊急使用授權(EUA)。食藥處表示,這將是南韓首次投入使用新冠口服藥,且首批藥物最快在明年1月下旬就會到貨。
根據《韓聯社》報導,南韓疾病管理廳22日向食藥處申請「Paxlovid」的緊急使用授權審查。考量到國內確診病例增加,使用口服藥治療的必要性提升、對藥物安全性和效果的研究、專家諮詢會議等結果,並經過相關單位的委員會審議後,決定批准該款口服藥的緊急使用授權。

據了解,雖然南韓18歲以上人口的疫苗覆蓋率高達92%,但是自從11月初開始鬆綁防疫規範,實施「分階段恢復日常」措施後,國內再掀感染潮,嚴重壓迫醫療量能,引進新冠口服藥進行治療的必要性也因此提升。
南韓食藥處在記者會中指出,Paxlovid有望避免住院或居家治療的新冠患者的病情出現嚴重惡化。預計將提供給病情有可能惡化為重症的12歲以上、體重超過40公斤的族群使用,需服用5天,每天2劑。孕婦只有在經評估後,服藥的作用「利大於弊」時才可開放,哺乳期的婦女則需在用藥後停止哺乳。

除此之外,早前實驗已證實Paxlovid對Omicron以外的變種病毒有效,該部門也預測Paxlovid對Omicron同樣存在抗菌作用。不過仍需等待輝瑞提供相關研究證明。
南韓疾病管理廳今日也同步公布新冠口服藥引進計劃,透露政府已與美國默沙東公司(MSD)和輝瑞公司分別簽下24.2萬人份和36.2萬人份的合約,首批藥物預計最快在明年1月中旬到貨。
《TVBS》提醒您:
因應新冠肺炎疫情,疾管署持續疫情監測與邊境管制措施,如有疑似症狀,請撥打:1922專線,或 0800-001922。
◤日本旅遊必買清單◢