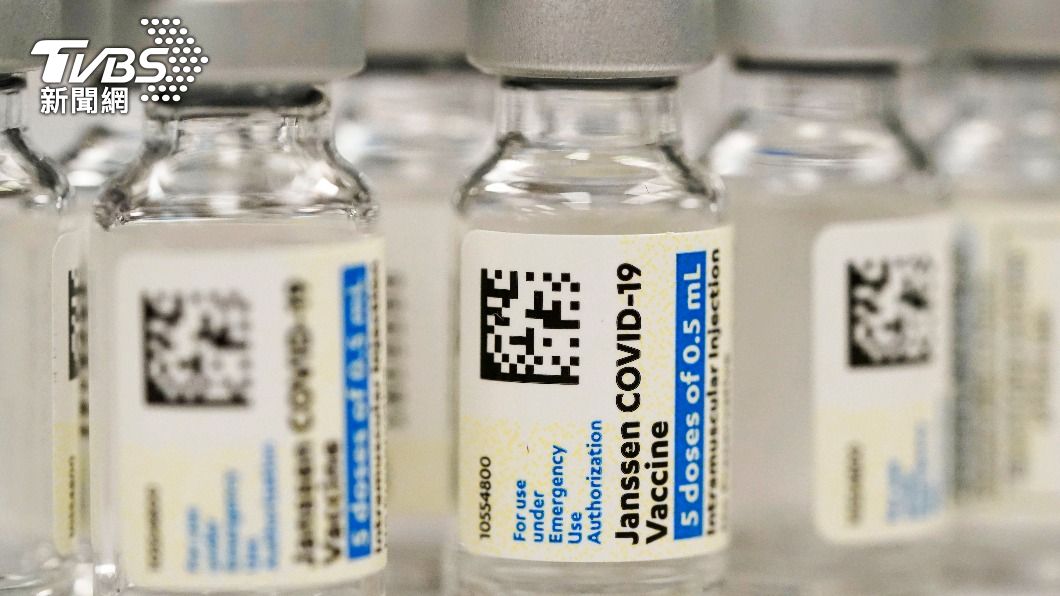
美國食品暨藥物管理局(FDA)5日宣布,考慮到接種嬌生(Johnson & Johnson)新冠疫苗恐引發罕見但嚴重血栓的風險,將對緊急使用授權範圍進行限制,即嬌生疫苗僅給不適合其他疫苗、無法取得疫苗以及選擇特定疫苗的18歲以上成年人施打。
《紐約時報》報導,美國FDA表示,接種嬌生疫苗的約1800萬劑中,有60例出現罕見且嚴重的「凝血狀況」,即血栓併血小板低下症候群(Thrombosis with Thrombocytopenia Syndrome,TTS),其中有9例死亡。

在衡量過接種嬌生的風險和益處後,FDA決定將其施打範圍限制在無法取得mRNA疫苗(輝瑞或莫德納)的成年人、對mRNA疫苗(如輝瑞或莫德納等疫苗)有嚴重過敏反應的成年人、或是對mRNA疫苗有個人擔憂(如果沒有嬌生疫苗就不會接種疫苗)的成年人。
美國疾病管制預防中心(CDC)在去年12月就已建議美國民眾,由於罕見的血栓案例,優先選擇輝瑞和莫德納的mRNA疫苗,理由是好處更多、風險更低。

FDA生物製品評估和研究中心主任馬克斯(Peter Marks)表示,「嬌生新冠疫苗在當前美國和全球新冠疫情大流行應對中仍然發揮作用,今天的決定反映FDA對接種此疫苗後TTS風險的最新分析,並將疫苗使用限定在某些人身上。我們一直在密切監測嬌生疫苗和TTS發生情況,採用安全監測系統的最新資訊修訂緊急授權(EUA)」。
◤日本旅遊必買清單◢