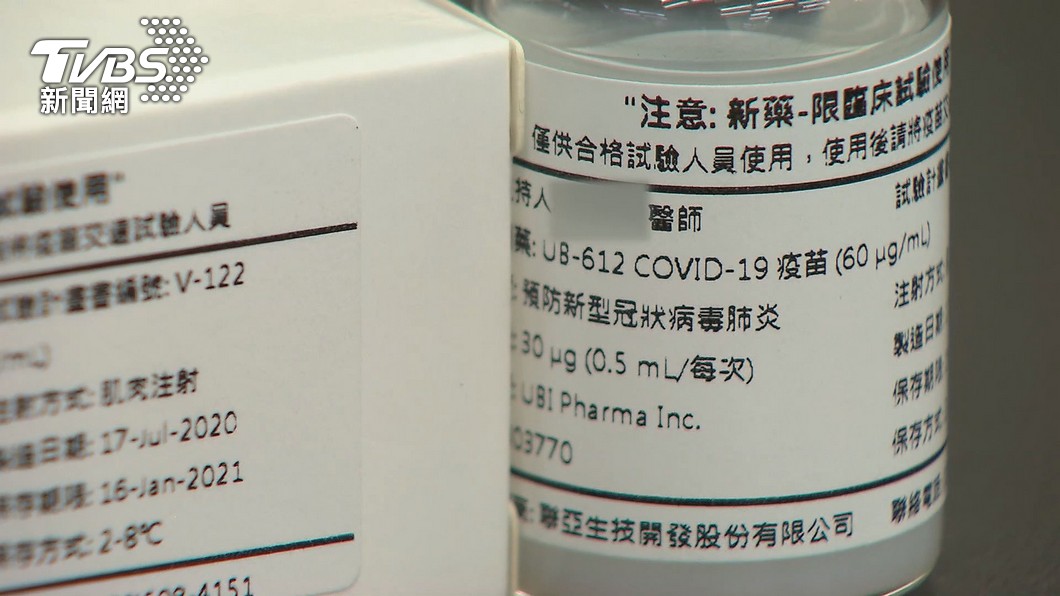
聯亞生技表示,近期將提50名受試者追加第3劑疫苗的新數據再度申請EUA。衛福部食藥署長吳秀梅今天坦言「有困難」,因受試者數目較少,將等聯亞送件再檢視。
中央流行疫情指揮中心8月16日宣布,聯亞生技研發的COVID-19(2019冠狀病毒疾病)疫苗,因中和抗體效價與血清反應數據未達標準,未通過衛生福利部食品藥物管理署緊急使用授權(EUA)審查。
聯亞昨天表示,50名第1期臨床試驗受試者接種2劑聯亞的COVID-19疫苗後8到10個月,再追加第3劑疫苗,結果顯示,對武漢病毒株及最早在印度發現的Delta變異株均產生高度中和抗體效價。
聯亞表示,近期將提送新數據至衛福部食藥署,申請緊急使用授權(EUA)再審。
吳秀梅今天上午接受媒體電話聯訪,針對聯亞將提再審EUA,坦言「有困難」,因受試者數目很少,不一定能說服審查委員。
吳秀梅說,提出EUA再審是人民的權利,但截至中午她尚未看見聯亞提資料送審,若聯亞未來送件,食藥署就會檢視資料,現在說還言之過早。(中央社)
《TVBS》提醒您:
因應新冠肺炎疫情,疾管署持續疫情監測與邊境管制措施,如有疑似症狀,請撥打:1922專線,或 0800-001922。
◤2024史上最熱一年◢