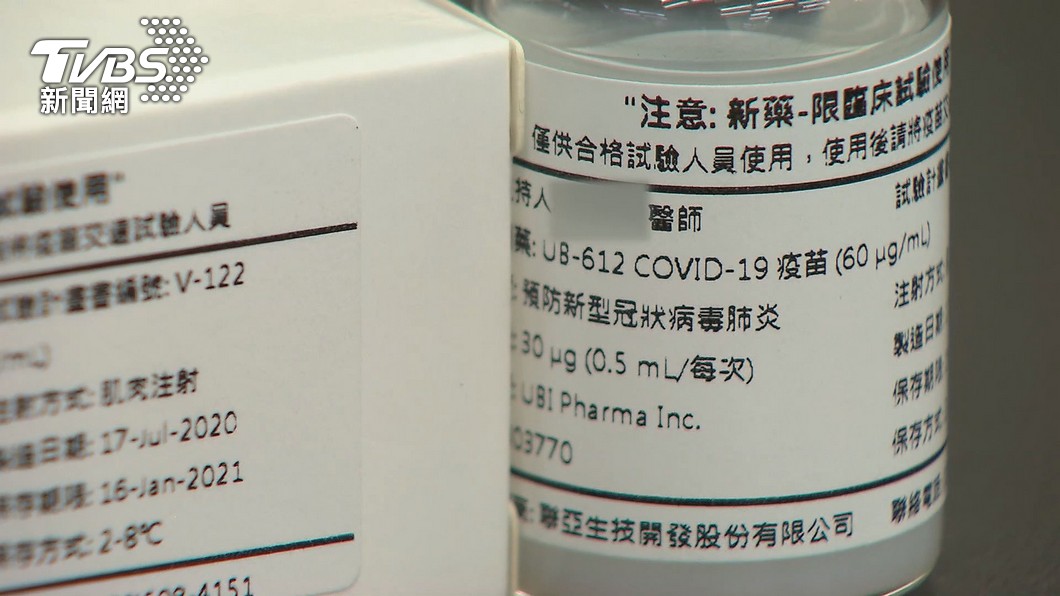
繼高端之後,國產疫苗另一家廠商聯亞今(27)日晚間6點也公布二期臨床試驗解盲結果,聯亞行政管理中心副總經理暨發言人范瀛云指出,聯亞生技新冠疫苗的UB-612,在不分年齡層組在接種2劑過後,血清陽轉率高達95.65%,中和抗體效價合乎預期,同時沒有出現嚴重不良反應。
聯亞行政管理中心副總經理暨發言人范瀛云,表示在第2劑施打後28天,血清陽轉率成年組(19至64歲)95.65%,65歲以上88.57,中和抗體效價為102.3,符合EUA標準。
此外局部不良反應部分,疫苗組注射部位疼痛64.59%,腫脹34.06%,全身性不良反應,疫苗組則發燒的只有1.93%、疲倦肌肉疼痛比例超過3成,頭痛的比率為17.01%,1成人有腹瀉。
效力部分因為不是三期,所以無法提供保護率資訊,但是透過血清陽轉率和中和抗體效價比較代表可以提供保護。聯亞生技創辦人王長怡日前估計,疫苗保護力粗估有望達到90%上下。

聯亞在2月7日時公布的第一期臨床試驗結果,顯示出高劑量組之中和抗體效價在施打第二劑後14及28天之血清陽轉率達100%,而中和抗體之幾何平均效價,增加40倍以上,當時就認為此疫苗有良好的安全性及耐受性,和優異免疫原性反應。
UB-612是COVID-19多重表次單位疫苗,業者指出,有針對新冠病毒有精準設計,可以活化並引發T細胞之記憶反應和效用功能,提高疫苗的有效性、安全性並避免不必要的免疫反應與副作用,也不需要以超低溫冷鏈運送及儲存。

在二期臨床試驗結果出爐以後,聯亞也會將把資料整理過後,送交食藥署審核緊急使用授權。聯亞估計若7月順利取得緊急使用授權,可以先提供2~3千劑疫苗,今年產能上看1~1.2億劑。
此外聯亞也透過關連公司Vaxxinity,已經在疫情嚴峻的印度申請要進行第三期臨床試驗,預計收納1.1萬人,以安慰劑對照組的試驗,也已經通報到WHO,拿到國際認證應該沒有問題。
《TVBS》提醒您:
因應新冠肺炎疫情,疾管署持續疫情監測與邊境管制措施,如有疑似症狀,請撥打:1922專線,或 0800-001922。